Indhold
- Hovedforskel
- Hemoglobin vs. Myoglobin
- Sammenligningstabel
- Hvad er hæmoglobin?
- typer
- Hvad er Myoglobin?
- Vigtige forskelle
- Konklusion
Hovedforskel
Den største forskel mellem hæmoglobin og myoglobin er, at hæmoglobin er et globinprotein, der overfører ilt til alle dele af organismens krop, mens myoglobin er et globinprotein, der kun overfører ilt til muskelceller.
Hemoglobin vs. Myoglobin
Respiration er en grundlæggende process i livet. Næsten hver organisme kræver transport af ilt til alle kroppens celler for at overleve. Hemoglobin og myoglobin er to basale globinproteiner i levende organismer, der binder ilt og overfører dem til cellerne. Men der findes en række forskelle mellem dem. Hemoglobin overfører ilt fra lungerne til alle kroppens dele eller celler i hvirveldyrene samt til nogle hvirvelløse dyr, mens myoglobin kun overfører ilt til muskelceller. Hemoglobin er sammensat af 4 polypeptidkæder, mens myoglobin er sammensat af den enkelte polypeptidkæde. Hæmoglobin findes i blodbanen, mens myoglobin findes i muskelceller.
Sammenligningstabel
| Hæmoglobin | myoglobin |
| Hemoglobin er et globinprotein, der overfører ilt fra lungerne til alle dele af kroppen. | Myoglobin er et globinprotein, der overfører ilt til muskelcellerne. |
| Struktur | |
| Det har en tetramer-struktur. | Det har en monomerstruktur. |
| Kæde | |
| Det er sammensat af 4 kæder af to forskellige typer, dvs. alpha og beta, delta, gamma eller epsilon (på typebasis af forskellige typer af hæmoglobin). | Den er sammensat af den enkelte polypeptidkæde. |
| Beliggenhed | |
| Det er placeret i hele kroppen. | Det er placeret i muskelceller. |
| Evne til at binde | |
| Det har evnen til at binde med CO2, NO, CO, O2 og H + | Det har evnen til at binde sig til O2 |
| Antal Hemes | |
| Det har fire hængsler, en i hver af underenhederne | Der er en heme i myoglobin |
| Antal iltmolekyler | |
| Fire iltmolekyler kan binde til hæmoglobin | Enkelt iltmolekyle binder til myoglobin |
| Molekylær vægt | |
| Dets molekylvægt er 64 kDa | Dets molekylvægt er 16,7 kDa |
| Affinitet til at binde med ilt | |
| Det har lav affinitet til at binde med ilt | Myoglobin har en høj affinitet til at binde med ilt |
| Koncentration i blod | |
| Det har en høj koncentration i røde blodlegemer | Det har en lav koncentration i blodet |
| Kurve | |
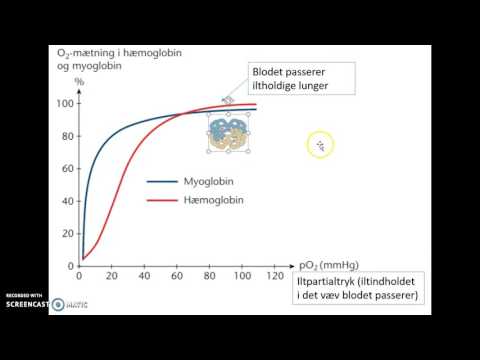
| Det viser sigmoid-bindingskurven | Det viser den hyperboliske kurve |
| Også kendt som | |
| Det er også kendt som Hb | Det er også kendt som Mb |
| Fungere | |
| Hemoglobin binder ilt og transporteres til alle dele af kroppen gennem blod. | Myoglobin overfører kun ilt til muskelceller, hvilket giver hjælp på sulten af ilt. |
Hvad er hæmoglobin?
Hemoglobin er et globeinprotein med flere underenheder med en kvartær struktur og består af fire polypeptidkæder, to a og to ß underenheder. Hver alfakæde består af 144 rester, og hver betakæde består af 146 rester. Modsætningerne underenheder som alfa og beta associeres stærkere end lignende underenheder alfa-alfa eller beta-beta. Det er et jernholdigt metalloprotein. I hæmoglobin er hver af de fire underenheder knyttet til en ikke-protein, protetisk hæmgruppe, hvor iltmolekylet binder. Så det betyder, at hæmoglobin kan binde fire iltmolekyler med fire hæmmegrupper i hver kæde. Det har lav iltaffinitet i sin deoxygenerede tilstand, men når først iltmolekylet binder til hæmoglobin fører det til ændringen i dets struktur, der gør bindingen af andre iltmolekyler lettere. Denne proces kaldes en allosterisk (gennem rum) interaktion / kooperativitet. Hemoglobin findes i overskydende i røde blodlegemer og giver dem en rød farve. Det involverer i transporten af ilt og kuldioxid til eller fra alle dele af kroppen. Det involverer også metabolisme af erythrocytter og opretholder også pH i blodet.
typer
- Hemoglobin A1 (Hb-A1).
- Hemoglobin A2 (Hb-A2).
- Hemoglobin A3 (Hb-A3).
- Embryonisk hæmoglobin.
- Glykosyleret hæmoglobin.
- Fosterhemoglobin (Hb-A1).
Hvad er Myoglobin?
Myoglobin er et monomer globinprotein, der udviser sekundær struktur. Den er sammensat af en enkelt polynukleotidkæde, der er sammensat af 153 rester. Det har en enkelt hammegruppe, der er knyttet til sin enkelt polypeptidkæde. Så et enkelt iltmolekyle kan binde til det. Men dens bindingsevne er højere end hæmoglobin, så det fungerer som et iltlagringsprotein, som frigøres under muskelfunktion. Det findes i muskelceller og leverer ilt til dem efter behov. Det hjælper kroppen ved sulten af ilt, især under de anaerobe forhold. Det regulerer også kropstemperatur. Myoglobin har ikke nogen type.
Vigtige forskelle
- Hemoglobin er et globinprotein, der overfører ilt fra lungerne til alle dele af kroppen, mens myoglobin er et globinprotein, der kun overfører ilt til muskelcellerne.
- Hemoglobin har en tetramerstruktur, mens myoglobin er en monomer i struktur.
- Hemoglobin består af 4 polypeptidkæder, hvorimod myoglobin er sammensat af den enkelte polypeptidkæde.
- Hemoglobin findes i røde blodlegemer, mens myoglobin findes i muskler
- Hemoglobin har fire hæmmegrupper, så det kan binde fire iltmolekyler, men myoglobin har en enkelt hæmmgruppe, så det kan binde et enkelt iltmolekyle, fordi hæmgruppe er stedet for binding af ilt
- Haemoglobin kan bindes med O2, CO2, CO, NO, BPH og H +, mens myoglobin kun kan binde med O2.
- Hemoglobin har 64 kDa molekylvægt, mens myoglobin har en molekylvægt på 16,7 kDa.
- Hemoglobin har en lav affinitet til at binde med ilt, mens myoglobin har en høj affinitet til at binde med ilt.
- Hemoglobin involverer i transporten af ilt og kuldioxid til eller fra alle dele af kroppen, i metabolismen af erythrocytter og opretholder også pH-værdien i blod, mens myoglobin findes i muskelceller og leverer ilt til dem på kravet og regulerer også kropstemperatur.
Konklusion
Fra ovenstående diskussion konkluderes det, at hæmoglobin er en tetramer sammensat af fire polynukleotidkæder og transporterer ilt og kuldioxid til alle dele af kroppen, mens myoglobin er en monomer sammensat af en enkelt nukleotidkæde og kun transporterer ilt til muskelceller efter behov .


